Analise da 7ª Reunião Extraordinária da Diretoria Colegiada
Análise da 7ª Reunião Extraordinária da Diretoria Colegiada (DICOL)
O M3BS, com o compromisso de levar conhecimento regulatório aos seus clientes faz acompanhamento de todas as reuniões técnicas da Agência Nacional de Saúde Suplementar (ANS), considerando que é por meio desses encontros que a reguladora especifica pontos importantes a serem trabalhados no setor, os quais vão muito além daqueles já previstos nos normativos vigentes e podem contribuir com a antecipação dos riscos e vantagens do mercado.
Desta forma, sobre a 7ª Reunião Extraordinária da DICOL, realizada em 08 de maio de 2026, o M3BS pontua sua análise, contendo, a seguir: (i) sumário executivo e (ii) descrição aprofundada dos itens de pauta.
SUMÁRIO EXECUTIVO:
Na 7ª Reunião Extraordinária da DICOL, foram deliberados os seguintes temas:
- Apreciação da Nota Técnica de Recomendação Preliminar (NTRP) nº 23/2026/GCITS/GGRAS/DIRAD-DIPRO/DIPRO, com deliberação acerca da abertura de Consulta Pública e Audiência Pública para as UATs nº 187, 188 e 198, no âmbito da proposta de atualização do Rol de Procedimentos e Eventos em Saúde;
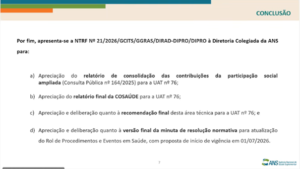
- Apreciação da Nota Técnica de Recomendação Final (NTRF) nº 21/2026/GCITS/GGRAS/DIRAD-DIPRO/DIPRO, referente à UAT nº 76, com deliberação sobre a atualização do Rol de Procedimentos e Eventos em Saúde para incorporação de exame diagnóstico relacionado à Síndrome Antifosfolipídica (SAF).
DESCRIÇÃO DOS ITENS DE PAUTA:
- Item 1 da DIPRO
DELIBERAÇÃO da proposta de atualização do Rol de Procedimentos e Eventos em Saúde. Abertura de Consulta Pública e Audiência Pública. Processo nº 33910.012010/2026-21.
Foi apreciada e deliberada a proposta de atualização do Rol de Procedimentos e Eventos em Saúde, consubstanciada na Nota Técnica de Recomendação Preliminar (NTRP) nº 23/2026/GCITS/GGRAS/DIRAD-DIPRO/DIPRO, referente às UATs nº 187, 188 e 198, nos termos do processo administrativo nº 33910.012010/2026-21.
No âmbito da referida Nota Técnica de Recomendação Preliminar, foram analisadas três tecnologias em saúde submetidas à avaliação técnica da ANS, com diferentes recomendações preliminares quanto à incorporação ao Rol de Procedimentos e Eventos em Saúde.
A primeira tecnologia avaliada refere-se à ablação percutânea por cateter de campo pulsado, indicada para o tratamento da fibrilação atrial paroxística (UAT nº 187), tendo sido apresentada recomendação preliminar favorável à incorporação.
A análise das evidências clínicas considerou dois ensaios clínicos randomizados de não inferioridade e uma revisão sistemática com metanálise, utilizando como comparador as técnicas convencionais de ablação térmica, incluindo radiofrequência e crioablação. Os resultados apontaram tendência favorável à tecnologia quanto à recorrência da fibrilação atrial, bem como redução de hospitalizações e visitas à emergência, embora sem diferenças estatisticamente significativas. A certeza da evidência foi classificada como moderada.
No tocante à segurança, observou-se tendência de menor risco de eventos adversos graves em comparação à ablação térmica, sem demonstração de superioridade clínica relevante. A conclusão técnica consignou que a tecnologia demonstrou não inferioridade em eficácia e segurança, sem comprovação suficiente de benefícios adicionais. Sob a perspectiva econômica, a avaliação indicou potencial de dominância, com melhor relação custo-resultado, impacto incremental considerado viável para a saúde suplementar e população-alvo estimada em aproximadamente 13.850 pacientes.
A segunda tecnologia analisada refere-se ao bimequizumabe para tratamento da hidradenite supurativa ativa moderada a grave em adultos que falharam, apresentaram intolerância ou contraindicação à terapia com antibióticos sistêmicos (UAT nº 188), tendo sido atribuída recomendação preliminar desfavorável à incorporação ao Rol.
A análise das evidências clínicas baseou-se em cinco revisões sistemáticas com comparações indiretas, utilizando como comparadores secuquinumabe e adalimumabe. Os resultados de curto prazo demonstraram evidência inconsistente, sem diferença estatisticamente significativa na maioria das análises, embora alguns estudos tenham indicado possível superioridade do bimequizumabe, considerada de baixa qualidade metodológica. Também foram apontadas diferenças metodológicas relevantes entre os estudos avaliados, além de aumento de eventos adversos associado ao uso da tecnologia.
Em relação aos resultados de longo prazo, verificaram-se indícios de superioridade em múltiplos desfechos clínicos, contudo a análise foi considerada limitada pela utilização de método indireto e pela qualidade metodológica criticamente baixa dos estudos. A avaliação econômica indicou dominância em relação ao adalimumabe, mas apresentou limitações relevantes quanto às premissas de participação de mercado, estimativas de utilidade e comparações de eficácia.
A terceira tecnologia apreciada refere-se ao capivasertibe em combinação com fulvestranto, indicado para tratamento de câncer de mama localmente avançado ou metastático, RH+ e HER2-, com uma ou mais alterações nos genes PIK3CA/AKT1/PTEN (UAT nº 198), tendo sido atribuída recomendação preliminar desfavorável à incorporação ao Rol.
A análise técnica considerou estudo clínico randomizado envolvendo pacientes em segunda linha de tratamento após progressão a inibidor de CDK4/6, utilizando fulvestranto isolado como comparador. Os resultados demonstraram benefício em sobrevida livre de progressão, com certeza de evidência considerada alta, além de possível redução do risco de morte, embora com baixa certeza da evidência quanto à sobrevida global.
No entanto, foram identificadas incertezas relevantes quanto aos impactos em qualidade de vida e resposta completa, ambas classificadas com baixo ou muito baixo grau de certeza da evidência. Também foram observados aumentos de eventos adversos gerais e graves associados ao tratamento combinado. A avaliação econômica apontou ganhos incrementais em anos de vida ganhos e qualidade de vida, porém destacou limitações relacionadas à utilização de utilidades provenientes de fontes externas, simplificações metodológicas e incerteza quanto à robustez dos resultados.
Diante das análises técnicas realizadas, foi deliberada a abertura de Consulta Pública, pelo prazo de 20 dias, no período de 13/05/2026 a 02/06/2026, para as UATs nº 187, 188 e 198, bem como a realização de Audiência Pública em 22/05/2026, especificamente em razão das recomendações preliminares desfavoráveis apresentadas para as UATs nº 188 e 198, nos termos da Lei nº 9.656/1998 e da RN/ANS nº 555/2022.
O item de pauta foi, assim, aprovado por unanimidade.
Seguem os slides apresentados:











2. Item 2 da DIPRO
DELIBERAÇÃO sobre tecnologias de saúde recomendadas positivamente pela Comissão Nacional de Incorporação de Tecnologia no Sistema Único de Saúde (CONITEC) para incorporação ao Sistema Único de Saúde. Processo nº 33910.006470/2024-59.
Deliberou-se sobre a proposta de atualização do Rol de Procedimentos e Eventos em Saúde, consubstanciada na Nota Técnica de Recomendação Final (NTRF) nº 21/2026/GCITS/GGRAS/DIRAD-DIPRO/DIPRO, referente à UAT nº 76, nos termos do processo administrativo nº 33910.006470/2024-59.
A proposta teve origem em recomendação da CONITEC, relacionada à incorporação de exames para prevenção de tromboembolismo venoso (TEV) em gestantes com trombofilia no âmbito do SUS, no período compreendido entre 02/05/2019 e 02/09/2021.
No contexto da análise regulatória realizada pela ANS, verificou-se que apenas um dos exames constantes dos relatórios da CONITEC ainda não possuía cobertura obrigatória na saúde suplementar, qual seja: anti-beta 2 glicoproteína I IgG e IgM, indicado para diagnóstico da Síndrome Antifosfolipídica (SAF).
A análise técnica destacou que a Síndrome Antifosfolipídica constitui importante trombofilia adquirida, associada ao aumento do risco de eventos trombóticos venosos e arteriais, bem como a desfechos obstétricos adversos, incluindo abortamento recorrente, pré-eclâmpsia precoce, restrição de crescimento intrauterino e falha em fertilização in vitro.
A recomendação final apresentada foi favorável à incorporação da tecnologia ao Rol de Procedimentos e Eventos em Saúde, com proposta de inclusão da DUT nº 174, prevendo cobertura obrigatória para diagnóstico da Síndrome Antifosfolipídica quando preenchido pelo menos um dos seguintes critérios clínicos:
- a) um ou mais episódios de trombose venosa ou arterial, comprovados por exame de imagem ou evidência histológica sem sinal de vasculite;
- b) histórico de, pelo menos, três abortamentos precoces, com menos de 10 semanas, sem causa aparente;
- c) histórico de óbito fetal com mais de dez semanas, com produto morfologicamente normal e sem causa aparente; ou
- d) histórico de parto prematuro antes de 34 semanas em razão de pré-eclâmpsia grave, eclâmpsia ou insuficiência placentária.
O percurso da tecnologia no rito processual compreendeu discussão inicial no âmbito da COSAÚDE, realização de Consulta Pública nº 164/2025, no período de 04 a 23/12/2025, bem como deliberação final após análise das contribuições da participação social ampliada na 50ª Reunião Técnica da COSAÚDE, realizada em abril de 2026.
Foi consignado, ainda, que a proposta de atualização do Rol prevê início de vigência em 01/07/2026.
O item de pauta foi, assim, aprovado por unanimidade.
Seguem os slides apresentados:






O M3BS faz o acompanhamento de todas as reuniões da Diretoria Colegiada da ANS para atualizar e manter o mercado informado sobre os principais pontos debatidos pela agência reguladora, além de orientar e antecipar os efeitos aplicáveis aos entes regulados frente as decisões tomadas pela agência.
Nosso time de especialistas pode atender sua necessidade! Contate-nos através do e-mail m3bsresponde@m3bs.com.br ou por telefone (11) 3115-2282.
Notícias Relacionadas
Mais Informações
MBS3 © Todos os direitos reservados.



