636ª Reunião DICOL – ANS
Análise da 636ª Reunião Ordinária da Diretoria Colegiada
O M3BS, com o compromisso de levar conhecimento regulatório aos seus clientes faz acompanhamento de todas as reuniões técnicas da Agência Nacional de Saúde Suplementar (ANS), considerando que é por meio desses encontros que a reguladora especifica pontos importantes a serem trabalhados no setor, os quais vão muito além daqueles já previstos nos normativos vigentes e podem contribuir com a antecipação dos riscos e vantagens do mercado.
Desta forma, sobre a 636ª Reunião da DICOL realizada em 24 de abril de 2026, o M3BS pontua sua análise, contendo, a seguir: (i) sumário executivo e (ii) descrição aprofundada dos itens de pauta:
SUMÁRIO EXECUTIVO:
Na 636ª Reunião Ordinária da Diretoria Colegiada da ANS, realizada em 24 de abril de 2026, foram deliberados os seguintes temas principais:
- Atualização do Rol – Recomendação Final (UAT nº 190)
A Diretoria de Normas e Habilitação dos Produtos (DIPRO) submeteu à deliberação a Nota Técnica de Recomendação Final referente à tecnologia Talazoparibe em combinação com Enzalutamida, tendo sido mantida recomendação desfavorável à incorporação ao Rol de Procedimentos e Eventos em Saúde. - Incorporação ao Rol de tecnologia recomendada pela CONITEC (Rituximabe)
A Diretoria Colegiada apreciou proposta de inclusão do medicamento Rituximabe para tratamento de Trombocitopenia Imune Primária, com atualização da respectiva Diretriz de Utilização.
DESCRIÇÃO DOS ITENS:
- Item extrapauta DIPRO
DELIBERAÇÃO sobre a proposta de atualização do Rol de Procedimentos e Eventos em Saúde. Retorno da Consulta Pública. Apreciação da Nota Técnica de Recomendação Final – NTRF referente à UAT nº 190. Processo nº 33910.000998/2026-86.
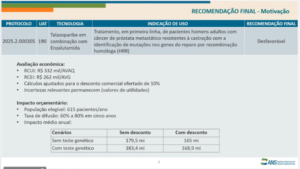
Trata-se da apreciação da Nota Técnica nº 20/2026/GCITS/GGRAS/DIRAD-DIPRO/DIPRO, que versa sobre a recomendação final quanto à incorporação da tecnologia Talazoparibe em combinação com Enzalutamida, indicada para tratamento, em primeira linha, de pacientes homens adultos com câncer de próstata metastático resistente à castração com identificação de mutações nos genes do reparo por recombinação homóloga (HRR).
O processo seguiu o rito regular de avaliação, com discussão inicial na 47ª Reunião Técnica da COSAÚDE, realização da Consulta Pública nº 167/2026 e Audiência Pública nº 63/2026, bem como nova análise após participação social ampliada na 49ª Reunião Técnica da COSAÚDE.
No mérito, a avaliação técnica considerou evidências clínicas baseadas em estudo fase III (TALAPRO-2), apontando redução no risco de morte e progressão da doença, bem como ganhos em sobrevida global e livre de progressão, ainda que acompanhados de aumento de eventos adversos graves e limitações metodológicas relevantes, especialmente quanto a vieses e inconsistências em desfechos de qualidade de vida.
Sob a perspectiva econômica, foram apresentados indicadores de custo-efetividade elevados, com incertezas relevantes, mesmo após aplicação de desconto comercial. O impacto orçamentário estimado indicou incremento significativo, com população elegível estimada em 615 pacientes por ano e impacto médio anual da ordem de R$ 165 milhões no cenário mais favorável.
Diante desse contexto, considerando a necessidade de sustentabilidade econômica da saúde suplementar, a área técnica manteve recomendação desfavorável à incorporação da tecnologia ao Rol.
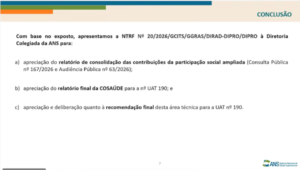
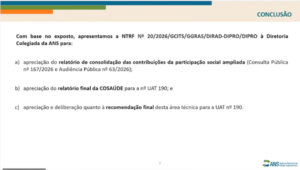
A Nota Técnica foi submetida à Diretoria Colegiada para: (i) apreciação do relatório de consolidação das contribuições da participação social; (ii) apreciação do relatório final da COSAÚDE; e (iii) deliberação quanto à recomendação final.
Seguem slides apresentados:





O item foi aprovado por unanimidade.
2. Item 2 extrapauta da DIPRO
DELIBERAÇÃO sobre Tecnologia em saúde recomendada positivamente pela Comissão Nacional de Incorporação de Tecnologias no Sistema Único de Saúde – CONITEC, para incorporação ao Sistema Único de Saúde – SUS. Tecnologia para incorporação ao Rol de Procedimentos e Eventos e Saúde. Processo nº 33910.000122/2026- 30.
Trata-se da apresentação da Nota Técnica nº 13/2026/GCITS/GGRAS/DIPRO, referente à análise de tecnologia recomendada positivamente pela CONITEC, com decisão de incorporação ao SUS e atualização de Protocolo Clínico e Diretrizes Terapêuticas (PCDT), para fins de avaliação quanto à inclusão no Rol de Procedimentos e Eventos em Saúde.
A análise foi realizada em cumprimento ao §10 do art. 10 da Lei nº 9.656/1998, que estabelece a obrigatoriedade de avaliação, no prazo de até 60 dias, das tecnologias incorporadas ao SUS para eventual inclusão na saúde suplementar, não tendo sido realizada análise de impacto orçamentário em razão da previsão legal de incorporação.
No caso concreto, trata-se do medicamento Rituximabe, indicado para tratamento de Trombocitopenia Imune Primária, cuja incorporação ao SUS foi acompanhada de atualização do respectivo PCDT, incluindo ampliação do público-alvo e ajustes na nomenclatura da doença.
Embora se trate de uso off-label em relação ao registro sanitário, a incorporação foi considerada possível em razão da recomendação da CONITEC e da publicação do PCDT pelo Ministério da Saúde.
Dessa forma, propôs-se: (i) a inclusão do medicamento Rituximabe no Rol de Procedimentos e Eventos em Saúde; e (ii) a atualização da Diretriz de Utilização (DUT nº 65), para contemplar sua indicação no tratamento da Trombocitopenia Imune Primária, especialmente em casos de doença persistente ou crônica e ausência de resposta ou contraindicação aos tratamentos de primeira linha.
Seguem slides apresentados:





O item foi aprovado por unanimidade.
O M3BS faz o acompanhamento de todas as reuniões da Diretoria Colegiada da ANS para atualizar e manter o mercado informado sobre os principais pontos debatidos pela agência reguladora, além de orientar e antecipar os efeitos aplicáveis aos entes regulados frente as decisões tomadas pela agência.
Nosso time de especialistas pode atender sua necessidade! Contate-nos através do e-mail m3bsresponde@m3bs.com.br ou por telefone (11) 3115-2282.
Notícias Relacionadas
Mais Informações
MBS3 © Todos os direitos reservados.



